Coenzimas
Las coenzimas son pequeñas moléculas orgánicas no proteicas que transportan grupos químicos entre las diferentes enzimas del organismo con el fin de favorecer la función de las mismas. También se les conoce como cosustratos.
Como bien indica este segundo nombre, las coenzimas no forman parte de las enzimas, sino que son sustratos que se unen a ellas. Debido a ello, se diferencian las coenzimas de los grupos no prostéticos de las enzimas, los cuales si se enlazan estrechamente a ellas.
Tanto las coenzimas como los grupos prostéticos pertenecen a un grupo más amplio, los llamados cofactores. Son moléculas no proteicas que necesitan a las enzimas para su actividad.
Las moléculas de coenzima son, a menudo, vitaminas, o se hacen a partir de vitaminas. Muchas coenzimas contienen el nucleótido adenosina como parte de su estructura. Un ejemplo de ello es el ATP, la coenzima A o el NAD+.
Un poco de historia sobre las coenzimas
La primera coenzima descubierta fue el NAD+, por Arthur Harder y William Youdin en el año 1906. Observaron que, añadiendo un extracto de levadura hervida y filtrada, la fermentación alcohólica en extracto de levadura sin hervir se aceleraba.
A principios del siglo XX, también se identificaron otras coenzimas como el ATP, por Karl Lohmann, y la coenzima A, por Fritz Albert Lipmann en el año 1945.
Quizá te interese: Dopamina
Funciones de las coenzimas
La principal función de las coenzimas es actuar como intermediarios metabólicos. Durante el metabolismo, se llevan a cabo numerosas reacciones bioquímicas. No obstante, la mayoría corresponden a unos tipos básicos de reacciones que implican la transferencia de grupos funcionales.
Cada clase de reacción de transferencia de grupo se realiza por una coenzima particular, que es el sustrato de un conjunto de enzimas que la producen y un conjunto de enzimas que la consumen.
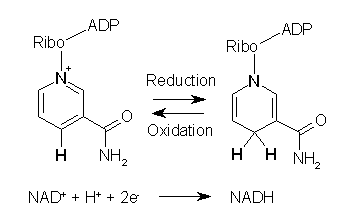
Un ejemplo de todo ello son las enzimas deshidrogenasas. Estas utilizan la NADH como cofactor. Cientos de enzimas diferentes eliminan los electrones de sus sustratos y reducen el NAD+ a NADH. Esta coenzima se reduce finalmente a un sustrato para cualquiera de las enzimas reductasas presentes en la célula que necesitan reducir sus sustratos.
Lee también: Endorfinas
Coenzimas más conocidas
A continuación, mencionamos algunas de las coenzimas más conocidas:
NAD+ y NADH
La nicotinamida adenina dinucleótido o NAD+ es una coenzima que se encuentra en todas las células vivas. Durante el metabolismo, participa en las reacciones redox, transportando los electrones de una reacción a otra.
De este modo, la coenzima se encuentra en dos formas en las células: NAD+ y NADH. La primera forma es el agente oxidante, ya que acepta electrones de otras moléculas y pasa a ser reducido formándose NADH, que se puede utilizar como agente reductor para donar electrones.
Coenzima A o CoA
La función principal de esta coenzima es la de transferir grupos acilo que participan en diversas rutas metabólicas, como en el ciclo de Krebs.
Está formada por tres partes:
- Cuerpo: formado por vitamina B5.
- Cabeza: compuesta por ADP o adenosina bifosfato.
- Cola: compuesta por beta-mercaptoetilamina.
La coenzima A ayuda a las enzimas a funcionar, pero también actúa como una especie de enlace para otras moléculas.
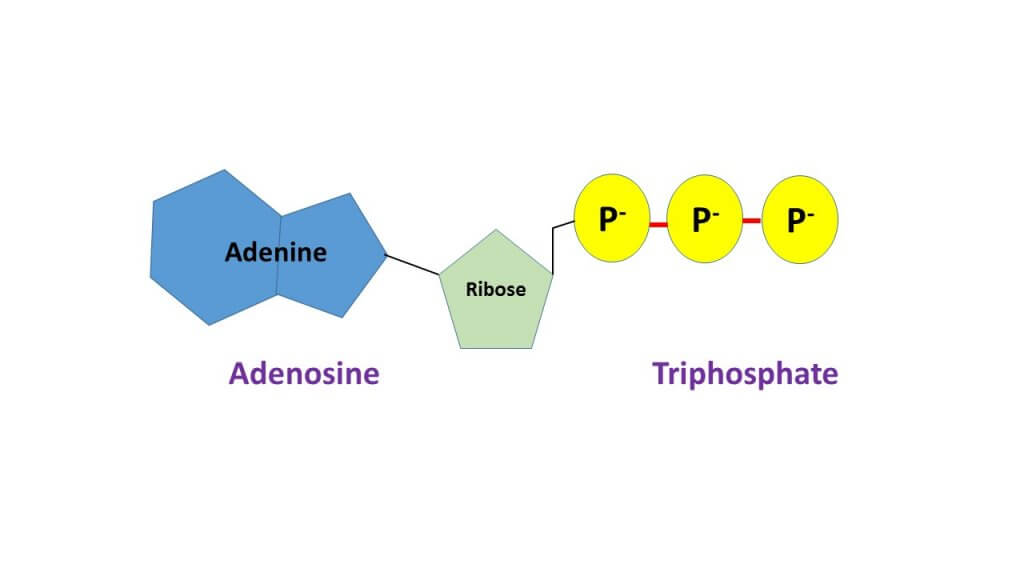
ATP o adenosina trifosfato
Se trata de una molécula utilizada por todos los organismos vivos para proporcionar energía en las reacciones químicas. Además, el ATP es el precursor de otras coenzimas, como las dos anteriores.
Es una coenzima muy importe, forma uno de los 4 monómeros utilizados en la síntesis de ARN celular.
Esta coenzima participa en la transferencia de los grupos metilo de las reacciones químicas. Fue descubierta por un italiano en el año 1952, Giulio Cantoni.
En su estructura se pueden encontrar ATP y metionina. Se han determinado más de 40 reacciones metabólicas que implican la transferencia de un grupo metilo desde la SAM a diferentes sustratos, como los ácidos nucleicos, proteínas y lípidos.
Glutatión
El glutatión o GSH es un tripéptido que contiene un enlace peptídico poco común entre el grupo amino de la cisteína y el grupo carboxilo de la cadena lateral de glutamato.
Es un antioxidante, por lo que protege a las células de toxinas y radicales libres. El glutatión se encuentra casi siempre en su forma reducida. La razón de ello es que la enzima que lo convierte a partir de su forma oxidada, la glutatión reductasa, es constitutivamente activa e inducible bajo estrés oxidativo.
Las coenzimas son pequeñas moléculas orgánicas no proteicas que transportan grupos químicos entre las diferentes enzimas del organismo con el fin de favorecer la función de las mismas. También se les conoce como cosustratos.
Como bien indica este segundo nombre, las coenzimas no forman parte de las enzimas, sino que son sustratos que se unen a ellas. Debido a ello, se diferencian las coenzimas de los grupos no prostéticos de las enzimas, los cuales si se enlazan estrechamente a ellas.
Tanto las coenzimas como los grupos prostéticos pertenecen a un grupo más amplio, los llamados cofactores. Son moléculas no proteicas que necesitan a las enzimas para su actividad.
Las moléculas de coenzima son, a menudo, vitaminas, o se hacen a partir de vitaminas. Muchas coenzimas contienen el nucleótido adenosina como parte de su estructura. Un ejemplo de ello es el ATP, la coenzima A o el NAD+.
Un poco de historia sobre las coenzimas
La primera coenzima descubierta fue el NAD+, por Arthur Harder y William Youdin en el año 1906. Observaron que, añadiendo un extracto de levadura hervida y filtrada, la fermentación alcohólica en extracto de levadura sin hervir se aceleraba.
A principios del siglo XX, también se identificaron otras coenzimas como el ATP, por Karl Lohmann, y la coenzima A, por Fritz Albert Lipmann en el año 1945.
Quizá te interese: Dopamina
Funciones de las coenzimas
La principal función de las coenzimas es actuar como intermediarios metabólicos. Durante el metabolismo, se llevan a cabo numerosas reacciones bioquímicas. No obstante, la mayoría corresponden a unos tipos básicos de reacciones que implican la transferencia de grupos funcionales.
Cada clase de reacción de transferencia de grupo se realiza por una coenzima particular, que es el sustrato de un conjunto de enzimas que la producen y un conjunto de enzimas que la consumen.
Un ejemplo de todo ello son las enzimas deshidrogenasas. Estas utilizan la NADH como cofactor. Cientos de enzimas diferentes eliminan los electrones de sus sustratos y reducen el NAD+ a NADH. Esta coenzima se reduce finalmente a un sustrato para cualquiera de las enzimas reductasas presentes en la célula que necesitan reducir sus sustratos.

Lee también: Endorfinas
Coenzimas más conocidas
A continuación, mencionamos algunas de las coenzimas más conocidas:
NAD+ y NADH
La nicotinamida adenina dinucleótido o NAD+ es una coenzima que se encuentra en todas las células vivas. Durante el metabolismo, participa en las reacciones redox, transportando los electrones de una reacción a otra.
De este modo, la coenzima se encuentra en dos formas en las células: NAD+ y NADH. La primera forma es el agente oxidante, ya que acepta electrones de otras moléculas y pasa a ser reducido formándose NADH, que se puede utilizar como agente reductor para donar electrones.
Coenzima A o CoA
La función principal de esta coenzima es la de transferir grupos acilo que participan en diversas rutas metabólicas, como en el ciclo de Krebs.
Está formada por tres partes:
- Cuerpo: formado por vitamina B5.
- Cabeza: compuesta por ADP o adenosina bifosfato.
- Cola: compuesta por beta-mercaptoetilamina.
La coenzima A ayuda a las enzimas a funcionar, pero también actúa como una especie de enlace para otras moléculas.
ATP o adenosina trifosfato
Se trata de una molécula utilizada por todos los organismos vivos para proporcionar energía en las reacciones químicas. Además, el ATP es el precursor de otras coenzimas, como las dos anteriores.
Es una coenzima muy importe, forma uno de los 4 monómeros utilizados en la síntesis de ARN celular.

Esta coenzima participa en la transferencia de los grupos metilo de las reacciones químicas. Fue descubierta por un italiano en el año 1952, Giulio Cantoni.
En su estructura se pueden encontrar ATP y metionina. Se han determinado más de 40 reacciones metabólicas que implican la transferencia de un grupo metilo desde la SAM a diferentes sustratos, como los ácidos nucleicos, proteínas y lípidos.
Glutatión
El glutatión o GSH es un tripéptido que contiene un enlace peptídico poco común entre el grupo amino de la cisteína y el grupo carboxilo de la cadena lateral de glutamato.
Es un antioxidante, por lo que protege a las células de toxinas y radicales libres. El glutatión se encuentra casi siempre en su forma reducida. La razón de ello es que la enzima que lo convierte a partir de su forma oxidada, la glutatión reductasa, es constitutivamente activa e inducible bajo estrés oxidativo.
- Vannucchi, H., & Monteiro, T. H. (2010). Ácido Fólico. ILSI Brasil.
- Comité de Medicamentos de la Asociación Española de Pediatria. (2012). Coenzima Q10 (Ubidecarenona). Piademecum.
- Patel, A., Malinovska, L., Saha, S., Wang, J., Alberti, S., Krishnan, Y., & Hyman, A. A. (2017). ATP as a biological hydrotrope. Science. https://doi.org/10.1126/science.aaf6846
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.