Distrofia muscular de Duchenne


Escrito y verificado por el biólogo Samuel Antonio Sánchez Amador
La distrofia muscular de Duchenne o DMD —por su traducción al inglés ‘Duchenne Muscular Dystrophy’— es una enfermedad hereditaria con un patrón de herencia recesivo. En líneas generales esta patología se caracteriza por una debilidad muscular rápida y progresiva que conduce a la muerte prematura del paciente.
Según estudios epidemiológicos, este grave trastorno se manifiesta en 7,1 hombres y 2,8 mujeres por cada 100 000 habitantes. Por baja que pueda parecer esta cifra, la prevalencia global indica que se trata de la enfermedad neuromuscular más frecuente y severa que se puede presentar durante la infancia.
Por esta razón, conocer las características y peculiaridades de la distrofia muscular de Duchenne se hace esencial. Hoy te presentamos todo lo que debes saber sobre ella, basándonos en bibliografía médica y estudios científicos. No te pierdas las siguientes líneas.
¿Qué es la distrofia muscular de Duchenne?
Como hemos dicho, la DMD es una enfermedad hereditaria marcada por una deficiencia muscular progresiva que empeora muy rápido. Según fuentes médicas, la causa directa de este suceso es una degeneración de los músculos lisos, esqueléticos y cardíacos. Veamos por qué.
El papel de la distrofina
La distrofina es una proteína citoesquelética que tiene como función prevenir el daño en la membrana de las células musculares —denominada sarcolema— durante el proceso de contracción muscular. A continuación te presentamos una serie de datos sobre la distrofina que nos ayudarán a entender la patología:
- Es una proteína estructural muscular codificada por el gen DMD. Se trata de la proteína más grande codificada en el genoma humano.
- Actúa como amortiguador a nivel tisular.
- Se une a la membrana del músculo y ayuda a mantener la estructura y organización de las células que lo conforman.
- Sin distrofina los músculos sufren daños progresivos hasta la muerte del tejido.
Portales especializados, como Duchenne Parent Project España ahondan un poco más en esta temática. Según sus hojas informativas, el daño en las membranas celulares musculares es un problema mayor, pues las sustancias fluyen dentro y fuera de estas estructuras de forma anómala.
Por ejemplo, la entrada de iones calcio a las células y fibras musculares —principales responsables de la contracción—, en ausencia de distrofina, puede provocar la liberación de enzimas y compuestos dañinos que causan perjuicio en los tejidos.
El efecto de la falta de distrofina
La entrada excesiva de iones calcio causa la ruptura de membranas, lo que permite la entrada de más calcio extracelular al interior de la célula a favor de gradiente. Es esperable que esta reacción en cascada promueva aún más la degradación muscular.
Al final, las células musculares destruidas son sustituidas por tejido conectivo fibroso y tejido adiposo, lo que causa una pérdida de función motora en el paciente. Estos espacios restringen el proceso de contracción muscular, llevando a la rigidez y deficiencia de funcionalidad muscular. En ausencia de distrofina se reduce la cantidad de células musculares y, las que quedan, van perdiendo su capacidad.
Causas de la DMD
Como hemos dicho, se trata de un trastorno genético recesivo. Se considera recesivo un alelo que solo se expresa con otro par igual a él. Pongamos un ejemplo:
- El alelo R codifica el color de ojos marrón y es de carácter dominante.
- El alelo r codifica el color de ojos azul y es recesivo.
Debemos tener en cuenta que un alelo es cada una de las formas alternativas de un gen y que —en genética típica— el individuo hereda dos de ellos para cada gen; uno del padre y otro de la madre. Así pues, las combinaciones posibles en este ejemplo serían RR, Rr y rr.
Según la definición antes expuesta, los ojos azules solo se expresarían en el genotipo rr, pues en el resto de casos el alelo marrón enmascararía la acción del azul, al ser este dominante. Con este ejemplo ficticio podemos entender un poco la herencia de la distrofia muscular de Duchenne.
Una enfermedad genética
En este caso, estamos ante una patología de carácter recesivo ligada al cromosoma X. El gen que codifica la distrofina se encuentra en el brazo corto del cromosoma X, más específicamente en el locus Xp21. Se trata de un gen grande, pues posee más de 2,5 millones de pares de bases y 79 regiones codificantes.
Dos tercios de los casos de DMD están asociados a la duplicación o eliminación de ciertos segmentos dentro de este gen, mientras que el porcentaje restante se debe a mutaciones puntuales demasiado pequeñas para ser detectadas. Esto, desde luego, tiene un efecto negativo durante el proceso de transcripción de ADN.
Sin entrar demasiado en materia, diremos que en condiciones normales el ARN mensajero lee el ADN y los genes de la célula y lleva la información a los ribosomas, donde se sintetiza la proteína codificada en el genoma. En este trastorno el marco de lectura que codifica a la distrofina se encuentra alterado, por lo que la síntesis de esta es imposible.
Según bases de datos genéticas de índole profesional, las estadísticas de las causas de la patología se distribuyen de la siguiente manera:
- Un 60-70 % de los enfermos muestran deleciones en el gen DMD. Esto quiere decir que se han eliminado ciertas secciones de material genético codificante como consecuencia de una mutación.
- Un 10 % de los pacientes muestran duplicaciones, es decir, repeticiones de información genética dentro del gen DMD.
- El 20 % restante de los casos se deben a pequeños errores.
Debido a los patrones de herencia genética, los hombres tienen muchas más probabilidades de sufrir la DMD que las mujeres.
Síntomas de la distrofia muscular de Duchenne
Una vez hemos aclarado las causas de la enfermedad, el siguiente paso es describir los síntomas de la distrofia muscular de Duchenne. Según la Biblioteca Nacional de Medicina de los Estados Unidos, estos primeros signos aparecen antes de los seis años de edad del paciente e, incluso, pueden mostrarse durante el periodo de lactancia.
Entre los síntomas de la patología encontramos los siguientes:
- Fatiga.
- Problemas de aprendizaje y discapacidad intelectual.
- Debilidad muscular: al correr y saltar, caídas frecuentes, dificultad para levantarse de una posición concreta y problemas respiratorios que empeoran.
- Dificultad progresiva para caminar: esta comienza hacia los 12 años de edad y las cardiopatías asociadas comienzan a manifestarse sobre los 20 años de vida.
En general, el diagnóstico puede demorarse hasta los 3-5 años de edad por la falta de signos diferenciables, pero a los 12 el infante suele requerir de una silla de ruedas para moverse. Por desgracia, la esperanza de vida media de los pacientes es de 30 años.
Diagnóstico
Para el diagnóstico de esta patología se requiere un examen completo del sistema nervioso, pulmones, corazón y músculos. Algunas pruebas a realizar son las siguientes:
- Electromiografía: técnica de registro gráfico de la actividad eléctrica presentada por los músculos.
- Pruebas de ADN: permiten detectar la mutación específica en la mayoría de los casos de DMD.
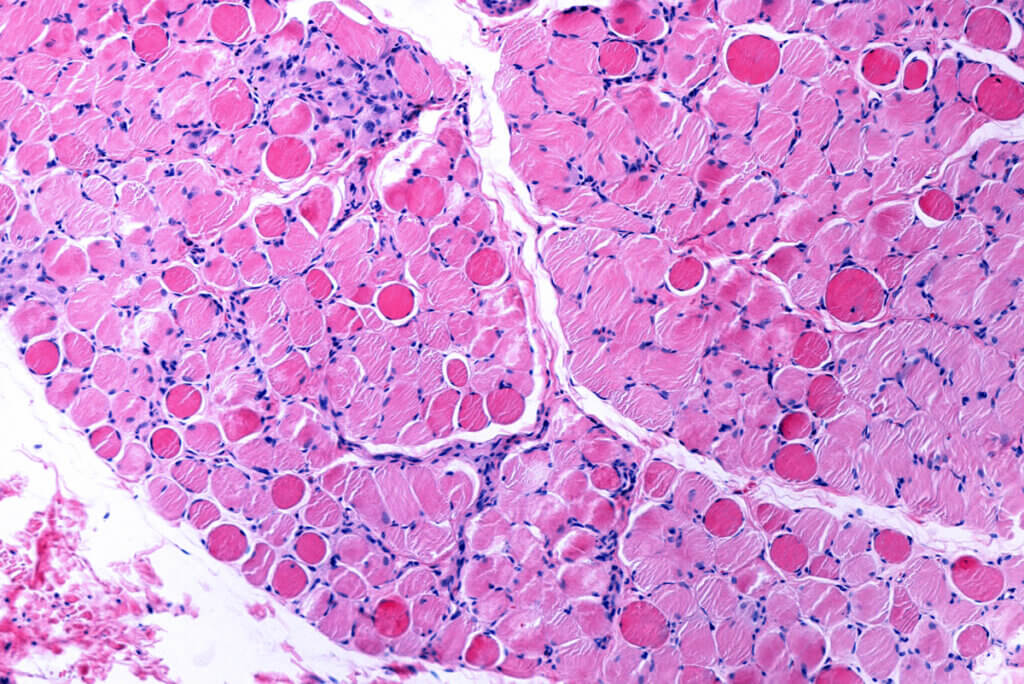
- Biopsia muscular: se puede obtener un pequeño segmento de tejido muscular en el que se buscará la proteína distrofina. Si está ausente, el diagnóstico está claro.
Un paciente con distrofia muscular de Duchenne mostrará pérdida de masa muscular, contracturas, deformidades, anormalidades cardíacas y trastornos respiratorios. Todos estos síntomas también pueden indicar al profesional que el cuadro general está causado por la DMD.

Tratamiento de la distrofia muscular de Duchenne
Hasta el año 2017 solo se planteaba un tratamiento paliativo para abordar la distrofia muscular de Duchenne. Es decir, brindarle la mejor existencia posible al paciente hasta que la enfermedad causara su muerte.
Esto puede incluir la ventilación asistida para ayudar al infante a respirar, fármacos para estabilizar la actividad cardíaca, aparatos ortopédicos y algunas cirugías puntuales para evitar una pérdida de movilidad completa. Por desgracia, sigue siendo un trastorno en el que la muerte solo es cuestión de tiempo.
También se pueden complementar estas medidas con esteroides, proteínas y vitaminas; sustancias administradas al paciente con el fin de enlentecer la distrofia muscular tan rápida que caracteriza a la enfermedad. Los efectos de estas terapias no son del todo efectivos.
Aún así, en tiempos recientes se ha comenzado a utilizar la terapia génica con el fin de abordar a los pacientes con DMD. Esta enfermedad ya se ha conseguido curar en ratones, perros y gatos y se encuentra en fase experimental en el ser humano. Desde luego, el futuro de este tratamiento es prometedor.
Esperanza para el futuro en la distrofia muscular de Duchenne
Como hemos podido ver en estas líneas, la enfermedad de Duchenne es un trastorno genético de progreso rápido, agresivo y con una tasa de supervivencia ínfima —casi todos los pacientes mueren antes de los 30 años de edad—. La distrofia muscular avanza y el enfermo suele fallecer por complicaciones cardíacas o respiratorias.
A pesar de los datos aquí expuestos, existe un rayo de esperanza, pues la terapia génica está reportando resultados muy prometedores en condiciones experimentales. Esperemos que sea solo una cuestión de tiempo.
La distrofia muscular de Duchenne o DMD —por su traducción al inglés ‘Duchenne Muscular Dystrophy’— es una enfermedad hereditaria con un patrón de herencia recesivo. En líneas generales esta patología se caracteriza por una debilidad muscular rápida y progresiva que conduce a la muerte prematura del paciente.
Según estudios epidemiológicos, este grave trastorno se manifiesta en 7,1 hombres y 2,8 mujeres por cada 100 000 habitantes. Por baja que pueda parecer esta cifra, la prevalencia global indica que se trata de la enfermedad neuromuscular más frecuente y severa que se puede presentar durante la infancia.
Por esta razón, conocer las características y peculiaridades de la distrofia muscular de Duchenne se hace esencial. Hoy te presentamos todo lo que debes saber sobre ella, basándonos en bibliografía médica y estudios científicos. No te pierdas las siguientes líneas.
¿Qué es la distrofia muscular de Duchenne?
Como hemos dicho, la DMD es una enfermedad hereditaria marcada por una deficiencia muscular progresiva que empeora muy rápido. Según fuentes médicas, la causa directa de este suceso es una degeneración de los músculos lisos, esqueléticos y cardíacos. Veamos por qué.
El papel de la distrofina
La distrofina es una proteína citoesquelética que tiene como función prevenir el daño en la membrana de las células musculares —denominada sarcolema— durante el proceso de contracción muscular. A continuación te presentamos una serie de datos sobre la distrofina que nos ayudarán a entender la patología:
- Es una proteína estructural muscular codificada por el gen DMD. Se trata de la proteína más grande codificada en el genoma humano.
- Actúa como amortiguador a nivel tisular.
- Se une a la membrana del músculo y ayuda a mantener la estructura y organización de las células que lo conforman.
- Sin distrofina los músculos sufren daños progresivos hasta la muerte del tejido.
Portales especializados, como Duchenne Parent Project España ahondan un poco más en esta temática. Según sus hojas informativas, el daño en las membranas celulares musculares es un problema mayor, pues las sustancias fluyen dentro y fuera de estas estructuras de forma anómala.
Por ejemplo, la entrada de iones calcio a las células y fibras musculares —principales responsables de la contracción—, en ausencia de distrofina, puede provocar la liberación de enzimas y compuestos dañinos que causan perjuicio en los tejidos.
El efecto de la falta de distrofina
La entrada excesiva de iones calcio causa la ruptura de membranas, lo que permite la entrada de más calcio extracelular al interior de la célula a favor de gradiente. Es esperable que esta reacción en cascada promueva aún más la degradación muscular.
Al final, las células musculares destruidas son sustituidas por tejido conectivo fibroso y tejido adiposo, lo que causa una pérdida de función motora en el paciente. Estos espacios restringen el proceso de contracción muscular, llevando a la rigidez y deficiencia de funcionalidad muscular. En ausencia de distrofina se reduce la cantidad de células musculares y, las que quedan, van perdiendo su capacidad.

Causas de la DMD
Como hemos dicho, se trata de un trastorno genético recesivo. Se considera recesivo un alelo que solo se expresa con otro par igual a él. Pongamos un ejemplo:
- El alelo R codifica el color de ojos marrón y es de carácter dominante.
- El alelo r codifica el color de ojos azul y es recesivo.
Debemos tener en cuenta que un alelo es cada una de las formas alternativas de un gen y que —en genética típica— el individuo hereda dos de ellos para cada gen; uno del padre y otro de la madre. Así pues, las combinaciones posibles en este ejemplo serían RR, Rr y rr.
Según la definición antes expuesta, los ojos azules solo se expresarían en el genotipo rr, pues en el resto de casos el alelo marrón enmascararía la acción del azul, al ser este dominante. Con este ejemplo ficticio podemos entender un poco la herencia de la distrofia muscular de Duchenne.
Una enfermedad genética
En este caso, estamos ante una patología de carácter recesivo ligada al cromosoma X. El gen que codifica la distrofina se encuentra en el brazo corto del cromosoma X, más específicamente en el locus Xp21. Se trata de un gen grande, pues posee más de 2,5 millones de pares de bases y 79 regiones codificantes.
Dos tercios de los casos de DMD están asociados a la duplicación o eliminación de ciertos segmentos dentro de este gen, mientras que el porcentaje restante se debe a mutaciones puntuales demasiado pequeñas para ser detectadas. Esto, desde luego, tiene un efecto negativo durante el proceso de transcripción de ADN.
Sin entrar demasiado en materia, diremos que en condiciones normales el ARN mensajero lee el ADN y los genes de la célula y lleva la información a los ribosomas, donde se sintetiza la proteína codificada en el genoma. En este trastorno el marco de lectura que codifica a la distrofina se encuentra alterado, por lo que la síntesis de esta es imposible.
Según bases de datos genéticas de índole profesional, las estadísticas de las causas de la patología se distribuyen de la siguiente manera:
- Un 60-70 % de los enfermos muestran deleciones en el gen DMD. Esto quiere decir que se han eliminado ciertas secciones de material genético codificante como consecuencia de una mutación.
- Un 10 % de los pacientes muestran duplicaciones, es decir, repeticiones de información genética dentro del gen DMD.
- El 20 % restante de los casos se deben a pequeños errores.
Debido a los patrones de herencia genética, los hombres tienen muchas más probabilidades de sufrir la DMD que las mujeres.
Síntomas de la distrofia muscular de Duchenne
Una vez hemos aclarado las causas de la enfermedad, el siguiente paso es describir los síntomas de la distrofia muscular de Duchenne. Según la Biblioteca Nacional de Medicina de los Estados Unidos, estos primeros signos aparecen antes de los seis años de edad del paciente e, incluso, pueden mostrarse durante el periodo de lactancia.
Entre los síntomas de la patología encontramos los siguientes:
- Fatiga.
- Problemas de aprendizaje y discapacidad intelectual.
- Debilidad muscular: al correr y saltar, caídas frecuentes, dificultad para levantarse de una posición concreta y problemas respiratorios que empeoran.
- Dificultad progresiva para caminar: esta comienza hacia los 12 años de edad y las cardiopatías asociadas comienzan a manifestarse sobre los 20 años de vida.
En general, el diagnóstico puede demorarse hasta los 3-5 años de edad por la falta de signos diferenciables, pero a los 12 el infante suele requerir de una silla de ruedas para moverse. Por desgracia, la esperanza de vida media de los pacientes es de 30 años.
Diagnóstico
Para el diagnóstico de esta patología se requiere un examen completo del sistema nervioso, pulmones, corazón y músculos. Algunas pruebas a realizar son las siguientes:
- Electromiografía: técnica de registro gráfico de la actividad eléctrica presentada por los músculos.
- Pruebas de ADN: permiten detectar la mutación específica en la mayoría de los casos de DMD.
- Biopsia muscular: se puede obtener un pequeño segmento de tejido muscular en el que se buscará la proteína distrofina. Si está ausente, el diagnóstico está claro.
Un paciente con distrofia muscular de Duchenne mostrará pérdida de masa muscular, contracturas, deformidades, anormalidades cardíacas y trastornos respiratorios. Todos estos síntomas también pueden indicar al profesional que el cuadro general está causado por la DMD.

Tratamiento de la distrofia muscular de Duchenne
Hasta el año 2017 solo se planteaba un tratamiento paliativo para abordar la distrofia muscular de Duchenne. Es decir, brindarle la mejor existencia posible al paciente hasta que la enfermedad causara su muerte.
Esto puede incluir la ventilación asistida para ayudar al infante a respirar, fármacos para estabilizar la actividad cardíaca, aparatos ortopédicos y algunas cirugías puntuales para evitar una pérdida de movilidad completa. Por desgracia, sigue siendo un trastorno en el que la muerte solo es cuestión de tiempo.
También se pueden complementar estas medidas con esteroides, proteínas y vitaminas; sustancias administradas al paciente con el fin de enlentecer la distrofia muscular tan rápida que caracteriza a la enfermedad. Los efectos de estas terapias no son del todo efectivos.
Aún así, en tiempos recientes se ha comenzado a utilizar la terapia génica con el fin de abordar a los pacientes con DMD. Esta enfermedad ya se ha conseguido curar en ratones, perros y gatos y se encuentra en fase experimental en el ser humano. Desde luego, el futuro de este tratamiento es prometedor.
Esperanza para el futuro en la distrofia muscular de Duchenne
Como hemos podido ver en estas líneas, la enfermedad de Duchenne es un trastorno genético de progreso rápido, agresivo y con una tasa de supervivencia ínfima —casi todos los pacientes mueren antes de los 30 años de edad—. La distrofia muscular avanza y el enfermo suele fallecer por complicaciones cardíacas o respiratorias.
A pesar de los datos aquí expuestos, existe un rayo de esperanza, pues la terapia génica está reportando resultados muy prometedores en condiciones experimentales. Esperemos que sea solo una cuestión de tiempo.
- Researchers Try to Update Prevalence of Duchenne Muscular Dystrophy, AJMC. Recogido a 1 de noviembre en https://www.ajmc.com/view/researchers-try-to-update-prevalence-of-duchenne-muscular-dystrophy
- Distrofia muscular de Duchenne, orphanet.org. Recogido a 1 de noviembre en https://www.orpha.net/consor/www/cgi-bin/OC_Exp.php?lng=ES&Expert=98896
- La proteína distrofina, Duchenne Parent Project España. Recogido a 1 de noviembre en https://www.duchenne-spain.org/la-distrofina/
- Delección, NIH. Recogido a 1 de noviembre en https://www.genome.gov/es/genetics-glossary/Delecion#:~:text=Una%20deleci%C3%B3n%20es%20un%20tipo,todo%20un%20fragmento%20de%20cromosoma.
- Homo sapiens dystrophin (DMD), RefSeqGene (LRG_199) on chromosome X, NCBI. Recogido a 1 de noviembre en https://www.ncbi.nlm.nih.gov/nuccore/256355061
- Distrofia muscular de Duchenne, Medlineplus.gov. Recogido a 1 de noviembre en https://medlineplus.gov/spanish/ency/article/000705.htm
- Bouwles, DE; McPhee SW, Li C, Gray SJ, Samulski JJ, Camp AS, Li J, Wang B, Monahan PE, Rabinowitz JE, Grieger JC, Govindasamy L, Agbandje-McKenna M, Xiao X, Samulski RJ. (febrero de 2012). «Phase 1 gene therapy for Duchenne muscular dystrophy using a translational optimized AAV vector.».
- Guiraud, Simon, and Kay E. Davies. "Pharmacological advances for treatment in Duchenne muscular dystrophy." Current opinion in pharmacology 34 (2017): 36-48.
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.