Coenzimi
I coenzimi sono piccole molecole organiche non proteiche che trasportano gruppi chimici tra i diversi enzimi del corpo per favorire le loro funzioni. Sono anche conosciuti come cosubstrati.
Come indica questo secondo nome, i coenzimi non fanno parte del gruppo degli enzimi, ma sono substrati che si legano ad essi. Si differenziano inoltre dai gruppi prostetici, molecole non proteiche che si legano più strettamente agli enzimi.
Sia i coenzimi che i gruppi prostetici appartengono a un gruppo più ampio, i cofattori. Sono entrambi molecole non proteiche che hanno bisogno di legarsi agli enzimi per svolgere la loro attività.
Le molecole di coenzima sono spesso vitamine o sono costituite da vitamine. Molti coenzimi contengono il nucleotide adenosina nella loro struttura. Un esempio di questo è l’ATP, il coenzima A o il NAD+.
Un po’ di storia sui coenzimi
Il primo coenzima scoperto fu il NAD+, da Arthur Harder e William Youdin nel 1906. Osservarono che aggiungendo estratto di lievito bollito e filtrato, la fermentazione alcolica nell’estratto di lievito non bollito veniva accelerata.
All’inizio del XX secolo furono identificati altri coenzimi, come l’ATP, da Karl Lohmann, e il coenzima A, da Fritz Albert Lipmann nel 1945.
Potrebbe interessarvi anche: Dopamina
Funzioni dei coenzimi
La funzione principale dei coenzimi è agire come intermediari metabolici. Nel metabolismo avvengono numerose reazioni biochimiche, tuttavia, la maggior parte corrisponde a modelli fondamentali di reazioni caratterizzati dal trasferimento di gruppi funzionali.
Ogni reazione di trasferimento di gruppo è svolta da uno specifico coenzima, che è il substrato per un insieme di enzimi che la producono e un insieme di enzimi che lo utilizzano.
Un esempio di questo sono gli enzimi deidrogenasi. Usano NADH come cofattore. Centinaia di enzimi diversi rimuovono gli elettroni dai loro substrati e riducono il NAD+ a NADH. Questo coenzima viene infine ridotto a substrato per uno qualsiasi degli enzimi reduttasi presenti nella cellula che devono ridurre i loro substrati.
Leggete anche: Endorfine
Coenzimi più conosciuti
Ecco alcuni dei coenzimi più conosciuti :
NAD+ e NADH
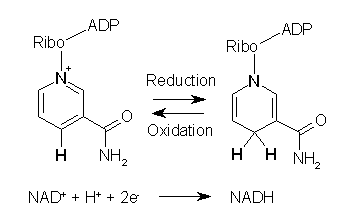
La nicotinammide adenina dinucleotide o NAD+ è un coenzima presente in tutte le cellule viventi. Durante il metabolismo partecipa alle reazioni redox, trasportando gli elettroni da una reazione all’altra.
Pertanto, il coenzima si trova in due forme nelle cellule: NAD + e NADH. La prima forma è l’agente ossidante, poiché accetta elettroni da altre molecole e si riduce, formando NADH, che può essere utilizzato come agente riducente per donare elettroni.
Coenzima A o CoA
La funzione principale di questo coenzima è quella di trasferire gruppi acilici che partecipano a varie vie metaboliche, come il ciclo di Krebs.
È composto da tre parti:
- Corpo: costituito da vitamina B5.
- Testa: composta da ADP o adenosina bisfosfato.
- Coda: composta da beta-mercaptoetilammina.
Il coenzima A aiuta gli enzimi a funzionare, ma agisce anche come collegamento per altre molecole.
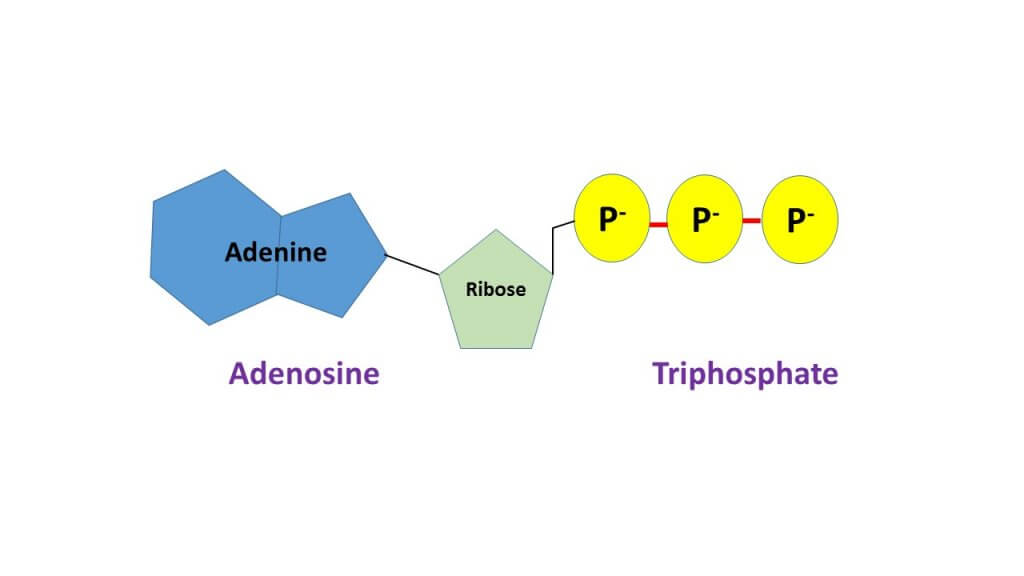
ATP o adenosina trifosfato
È una molecola utilizzata da tutti gli organismi viventi: fornisce energia nelle reazioni chimiche. Inoltre, l’ATP è il precursore di altri coenzimi, come i due precedenti.
È un coenzima molto importante, forma uno dei 4 monomeri utilizzati nella sintesi dell’RNA cellulare.
 SAM o S-adenosil metionina
SAM o S-adenosil metionina
Questo coenzima partecipa al trasferimento di gruppi metilici nelle reazioni chimiche. Fu scoperto da un italiano nel 1952, Giulio Cantoni.
Nella sua struttura si trovano ATP e metionina. Sono state determinate più di 40 reazioni metaboliche che comportano il trasferimento di un gruppo metilico da SAM a diversi substrati, come acidi nucleici, proteine e lipidi.
Glutatione
Il glutatione o GSH è un tripeptide che contiene un raro legame peptidico tra il gruppo amminico della cisteina e il gruppo carbossilico della catena laterale del glutammato.
È un antiossidante, quindi protegge le cellule dalle tossine e dai radicali liberi. Il glutatione è quasi sempre nella sua forma ridotta. La ragione di ciò è che l’enzima che lo converte dalla sua forma ossidata, la glutatione reduttasi, è costitutivamente attivo e inducibile sotto stress ossidativo.
I coenzimi sono piccole molecole organiche non proteiche che trasportano gruppi chimici tra i diversi enzimi del corpo per favorire le loro funzioni. Sono anche conosciuti come cosubstrati.
Come indica questo secondo nome, i coenzimi non fanno parte del gruppo degli enzimi, ma sono substrati che si legano ad essi. Si differenziano inoltre dai gruppi prostetici, molecole non proteiche che si legano più strettamente agli enzimi.
Sia i coenzimi che i gruppi prostetici appartengono a un gruppo più ampio, i cofattori. Sono entrambi molecole non proteiche che hanno bisogno di legarsi agli enzimi per svolgere la loro attività.
Le molecole di coenzima sono spesso vitamine o sono costituite da vitamine. Molti coenzimi contengono il nucleotide adenosina nella loro struttura. Un esempio di questo è l’ATP, il coenzima A o il NAD+.
Un po’ di storia sui coenzimi
Il primo coenzima scoperto fu il NAD+, da Arthur Harder e William Youdin nel 1906. Osservarono che aggiungendo estratto di lievito bollito e filtrato, la fermentazione alcolica nell’estratto di lievito non bollito veniva accelerata.
All’inizio del XX secolo furono identificati altri coenzimi, come l’ATP, da Karl Lohmann, e il coenzima A, da Fritz Albert Lipmann nel 1945.
Potrebbe interessarvi anche: Dopamina
Funzioni dei coenzimi
La funzione principale dei coenzimi è agire come intermediari metabolici. Nel metabolismo avvengono numerose reazioni biochimiche, tuttavia, la maggior parte corrisponde a modelli fondamentali di reazioni caratterizzati dal trasferimento di gruppi funzionali.
Ogni reazione di trasferimento di gruppo è svolta da uno specifico coenzima, che è il substrato per un insieme di enzimi che la producono e un insieme di enzimi che lo utilizzano.
Un esempio di questo sono gli enzimi deidrogenasi. Usano NADH come cofattore. Centinaia di enzimi diversi rimuovono gli elettroni dai loro substrati e riducono il NAD+ a NADH. Questo coenzima viene infine ridotto a substrato per uno qualsiasi degli enzimi reduttasi presenti nella cellula che devono ridurre i loro substrati.

Leggete anche: Endorfine
Coenzimi più conosciuti
Ecco alcuni dei coenzimi più conosciuti :
NAD+ e NADH
La nicotinammide adenina dinucleotide o NAD+ è un coenzima presente in tutte le cellule viventi. Durante il metabolismo partecipa alle reazioni redox, trasportando gli elettroni da una reazione all’altra.
Pertanto, il coenzima si trova in due forme nelle cellule: NAD + e NADH. La prima forma è l’agente ossidante, poiché accetta elettroni da altre molecole e si riduce, formando NADH, che può essere utilizzato come agente riducente per donare elettroni.
Coenzima A o CoA
La funzione principale di questo coenzima è quella di trasferire gruppi acilici che partecipano a varie vie metaboliche, come il ciclo di Krebs.
È composto da tre parti:
- Corpo: costituito da vitamina B5.
- Testa: composta da ADP o adenosina bisfosfato.
- Coda: composta da beta-mercaptoetilammina.
Il coenzima A aiuta gli enzimi a funzionare, ma agisce anche come collegamento per altre molecole.
ATP o adenosina trifosfato
È una molecola utilizzata da tutti gli organismi viventi: fornisce energia nelle reazioni chimiche. Inoltre, l’ATP è il precursore di altri coenzimi, come i due precedenti.
È un coenzima molto importante, forma uno dei 4 monomeri utilizzati nella sintesi dell’RNA cellulare.
 SAM o S-adenosil metionina
SAM o S-adenosil metionina
Questo coenzima partecipa al trasferimento di gruppi metilici nelle reazioni chimiche. Fu scoperto da un italiano nel 1952, Giulio Cantoni.
Nella sua struttura si trovano ATP e metionina. Sono state determinate più di 40 reazioni metaboliche che comportano il trasferimento di un gruppo metilico da SAM a diversi substrati, come acidi nucleici, proteine e lipidi.
Glutatione
Il glutatione o GSH è un tripeptide che contiene un raro legame peptidico tra il gruppo amminico della cisteina e il gruppo carbossilico della catena laterale del glutammato.
È un antiossidante, quindi protegge le cellule dalle tossine e dai radicali liberi. Il glutatione è quasi sempre nella sua forma ridotta. La ragione di ciò è che l’enzima che lo converte dalla sua forma ossidata, la glutatione reduttasi, è costitutivamente attivo e inducibile sotto stress ossidativo.
- Vannucchi, H., & Monteiro, T. H. (2010). Ácido Fólico. ILSI Brasil.
- Comité de Medicamentos de la Asociación Española de Pediatria. (2012). Coenzima Q10 (Ubidecarenona). Piademecum.
- Patel, A., Malinovska, L., Saha, S., Wang, J., Alberti, S., Krishnan, Y., & Hyman, A. A. (2017). ATP as a biological hydrotrope. Science. https://doi.org/10.1126/science.aaf6846
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.