Que sont les coenzymes?

Les coenzymes sont de petites molécules organiques non protéiques qui transportent des groupes chimiques entre les différentes enzymes du corps afin de favoriser leur fonction. Elles sont également appelées cosubstrats.
Comme ce deuxième terme l’indique, les coenzymes ne font pas partie des enzymes, mais sont des substrats qui se lient à elles. Pour cette raison, les coenzymes des groupes non prothétiques se différencient en s’unissant étroitement à eux.
Les coenzymes et les groupes prothétiques appartiennent à un groupe plus large, les cofacteurs. Ce sont des molécules non protéiques qui ont besoin d’enzymes pour leur activité.
Par ailleurs, les molécules de coenzyme sont souvent des vitamines, ou sont fabriquées à partir de vitamines. De nombreuses coenzymes contiennent le nucléotide adénosine dans le cadre de leur structure. Un exemple de ceci est l’ATP, la coenzyme A ou le NAD +.
Un peu d’histoire sur les coenzymes
La première coenzyme découverte était le NAD +, par Arthur Harder et William Youdin en 1906. Ils ont observé qu’en ajoutant un extrait de levure bouillie et filtrée, la fermentation alcoolique en extrait de levure non bouillie était accélérée.
Au début du 20e siècle, d’autres coenzymes ont également été identifiées, telles que l’ATP, par Karl Lohmann, et la coenzyme A, par Fritz Albert Lipmann en 1945.
Cela pourrait vous intéresser : 7 astuces pour générer davantage de dopamine
Fonctions des coenzymes
La fonction principale des coenzymes est d’agir comme intermédiaires métaboliques. Au cours du métabolisme, de nombreuses réactions biochimiques ont lieu. Cependant, la plupart correspondent à des types basiques de réactions qui impliquent le transfert de groupes fonctionnels.
Chaque type de réaction de transfert de groupe est réalisé par une coenzyme particulière, qui est le substrat d’un ensemble d’enzymes qui le produisent et d’un ensemble d’enzymes qui le consomment.
Un exemple de tout cela sont les enzymes déshydrogénases. Elles utilisent le NADH comme cofacteur. Des centaines d’enzymes différentes retirent les électrons de leurs substrats et réduisent le NAD+ en NADH. Cette coenzyme est finalement réduite à un substrat pour l’une des enzymes réductases présentes dans la cellule qui doivent réduire leurs substrats.
A lire aussi : Endorphines: origine moléculaire, fonctions et mécanisme
Coenzymes les plus connues
Voici quelques-unes des coenzymes les plus connues :
NAD+ et NADH
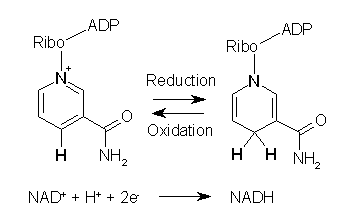
La nicotinamide adénine dinucléotide ou NAD+ est une coenzyme présente dans toutes les cellules vivantes. Au cours du métabolisme, elle participe aux réactions d’oxydoréduction, transportant des électrons d’une réaction à l’autre.
Ainsi, la coenzyme se retrouve sous deux formes dans les cellules : NAD + et NADH. La première forme est l’agent oxydant. Car il accepte les électrons d’autres molécules et se réduit, formant le NADH, qui peut être utilisé comme agent réducteur pour donner des électrons.
Coenzyme A ou CoA
La fonction principale de cette coenzyme est de transférer des groupes acyles qui participent à diverses voies métaboliques, telles que le cycle de Krebs.
Elle se compose de trois parties :
- Corps : composé de vitamine B5.
- Tête : composée d’ADP ou d’adénosine bisphosphate.
- Queue : composé de bêta-mercaptoéthylamine.
La coenzyme A aide les enzymes à fonctionner, mais elle agit également comme une sorte de lien pour d’autres molécules.
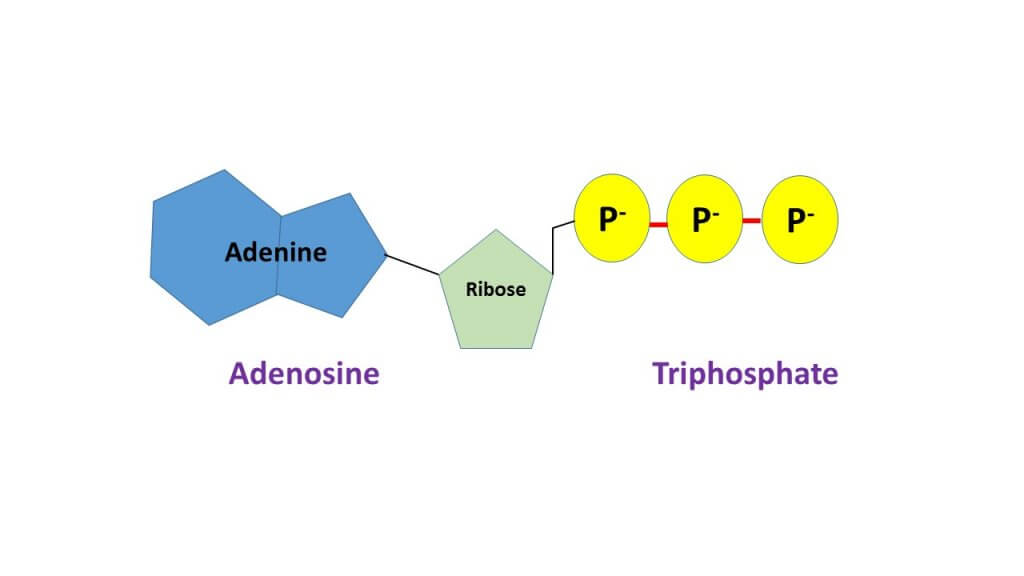
ATP ou adénosine triphosphate
C’est une molécule utilisée par tous les organismes vivants pour fournir de l’énergie dans les réactions chimiques. De plus, l’ATP est le précurseur d’autres coenzymes, comme les deux précédentes.
Il s’agit d’une coenzyme très importante. Elle forme l’un des 4 monomères utilisés dans la synthèse de l’ARN cellulaire.
 SAM ou S-adénosyl méthionine
SAM ou S-adénosyl méthionine
Cette coenzyme participe au transfert des groupements méthyle dans les réactions chimiques. Elle a été découverte par un Italien en 1952, Giulio Cantoni.
L’ATP et la méthionine peuvent être trouvés dans sa structure. Plus de 40 réactions métaboliques ont été déterminées qui impliquent le transfert d’un groupe méthyle de SAM vers différents substrats, tels que des acides nucléiques, des protéines et des lipides.
Glutathion
Le glutathion ou GSH est un tripeptide qui contient une liaison peptidique rare entre le groupe amino de la cystéine et le groupe carboxyle de la chaîne latérale du glutamate.
C’est un antioxydant, il protège donc les cellules des toxines et des radicaux libres. Le glutathion est presque toujours sous sa forme réduite. La raison en est que l’enzyme qui le convertit à partir de sa forme oxydée, la glutathion réductase, est constitutivement active et inductible sous stress oxydatif.
Les coenzymes sont de petites molécules organiques non protéiques qui transportent des groupes chimiques entre les différentes enzymes du corps afin de favoriser leur fonction. Elles sont également appelées cosubstrats.
Comme ce deuxième terme l’indique, les coenzymes ne font pas partie des enzymes, mais sont des substrats qui se lient à elles. Pour cette raison, les coenzymes des groupes non prothétiques se différencient en s’unissant étroitement à eux.
Les coenzymes et les groupes prothétiques appartiennent à un groupe plus large, les cofacteurs. Ce sont des molécules non protéiques qui ont besoin d’enzymes pour leur activité.
Par ailleurs, les molécules de coenzyme sont souvent des vitamines, ou sont fabriquées à partir de vitamines. De nombreuses coenzymes contiennent le nucléotide adénosine dans le cadre de leur structure. Un exemple de ceci est l’ATP, la coenzyme A ou le NAD +.
Un peu d’histoire sur les coenzymes
La première coenzyme découverte était le NAD +, par Arthur Harder et William Youdin en 1906. Ils ont observé qu’en ajoutant un extrait de levure bouillie et filtrée, la fermentation alcoolique en extrait de levure non bouillie était accélérée.
Au début du 20e siècle, d’autres coenzymes ont également été identifiées, telles que l’ATP, par Karl Lohmann, et la coenzyme A, par Fritz Albert Lipmann en 1945.
Cela pourrait vous intéresser : 7 astuces pour générer davantage de dopamine
Fonctions des coenzymes
La fonction principale des coenzymes est d’agir comme intermédiaires métaboliques. Au cours du métabolisme, de nombreuses réactions biochimiques ont lieu. Cependant, la plupart correspondent à des types basiques de réactions qui impliquent le transfert de groupes fonctionnels.
Chaque type de réaction de transfert de groupe est réalisé par une coenzyme particulière, qui est le substrat d’un ensemble d’enzymes qui le produisent et d’un ensemble d’enzymes qui le consomment.
Un exemple de tout cela sont les enzymes déshydrogénases. Elles utilisent le NADH comme cofacteur. Des centaines d’enzymes différentes retirent les électrons de leurs substrats et réduisent le NAD+ en NADH. Cette coenzyme est finalement réduite à un substrat pour l’une des enzymes réductases présentes dans la cellule qui doivent réduire leurs substrats.

A lire aussi : Endorphines: origine moléculaire, fonctions et mécanisme
Coenzymes les plus connues
Voici quelques-unes des coenzymes les plus connues :
NAD+ et NADH
La nicotinamide adénine dinucléotide ou NAD+ est une coenzyme présente dans toutes les cellules vivantes. Au cours du métabolisme, elle participe aux réactions d’oxydoréduction, transportant des électrons d’une réaction à l’autre.
Ainsi, la coenzyme se retrouve sous deux formes dans les cellules : NAD + et NADH. La première forme est l’agent oxydant. Car il accepte les électrons d’autres molécules et se réduit, formant le NADH, qui peut être utilisé comme agent réducteur pour donner des électrons.
Coenzyme A ou CoA
La fonction principale de cette coenzyme est de transférer des groupes acyles qui participent à diverses voies métaboliques, telles que le cycle de Krebs.
Elle se compose de trois parties :
- Corps : composé de vitamine B5.
- Tête : composée d’ADP ou d’adénosine bisphosphate.
- Queue : composé de bêta-mercaptoéthylamine.
La coenzyme A aide les enzymes à fonctionner, mais elle agit également comme une sorte de lien pour d’autres molécules.
ATP ou adénosine triphosphate
C’est une molécule utilisée par tous les organismes vivants pour fournir de l’énergie dans les réactions chimiques. De plus, l’ATP est le précurseur d’autres coenzymes, comme les deux précédentes.
Il s’agit d’une coenzyme très importante. Elle forme l’un des 4 monomères utilisés dans la synthèse de l’ARN cellulaire.
 SAM ou S-adénosyl méthionine
SAM ou S-adénosyl méthionine
Cette coenzyme participe au transfert des groupements méthyle dans les réactions chimiques. Elle a été découverte par un Italien en 1952, Giulio Cantoni.
L’ATP et la méthionine peuvent être trouvés dans sa structure. Plus de 40 réactions métaboliques ont été déterminées qui impliquent le transfert d’un groupe méthyle de SAM vers différents substrats, tels que des acides nucléiques, des protéines et des lipides.
Glutathion
Le glutathion ou GSH est un tripeptide qui contient une liaison peptidique rare entre le groupe amino de la cystéine et le groupe carboxyle de la chaîne latérale du glutamate.
C’est un antioxydant, il protège donc les cellules des toxines et des radicaux libres. Le glutathion est presque toujours sous sa forme réduite. La raison en est que l’enzyme qui le convertit à partir de sa forme oxydée, la glutathion réductase, est constitutivement active et inductible sous stress oxydatif.
- Vannucchi, H., & Monteiro, T. H. (2010). Ácido Fólico. ILSI Brasil.
- Comité de Medicamentos de la Asociación Española de Pediatria. (2012). Coenzima Q10 (Ubidecarenona). Piademecum.
- Patel, A., Malinovska, L., Saha, S., Wang, J., Alberti, S., Krishnan, Y., & Hyman, A. A. (2017). ATP as a biological hydrotrope. Science. https://doi.org/10.1126/science.aaf6846
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.